Bài báo cáo gửi ngày 2 tháng 6 năm 2017; được xem xét vào ngày 15 tháng 8 năm 2017; được chấp nhận đăng vào ngày 22 tháng 8 năm 2017.
Thông điệp lâm sàng chính
Một bệnh nhân bị ung thư biểu mô đường tiết niệu trên đa di căn (Upper tract urothelial carcinoma - UTUC) kháng hóa trị nay được điều trị bằng duy nhất liệu pháp vắc-xin khối u tự thân cố định bằng formallin (AFTV) đã dẫn đến sự thuyên giảm hoàn toàn di căn ở phổi và hạch bạch huyết cạnh động mạch chủ (liên tục > 3 năm sau khi làm AFTV). Miễn dịch học của khối u âm tính với PD-L1. AFTV sẽ là một lựa chọn điều trị hấp dẫn.
Giới thiệu
Ung thư biểu mô đường tiết niệu trên (UTUC) là một bệnh hiếm gặp, chiếm 5% các bệnh ác tính ở niệu quản [1, 2]. Phẫu thuật cắt bỏ thận mở rộng (radical nephroureterectomy - RNU) với cắt bỏ chóp niệu quản - bàng quang được coi là tiêu chuẩn phẫu thuật điều trị cho UTUC không di căn. Tuy nhiên, khoảng 30% bệnh nhân tiến triển tái phát sau ca phẫu thuật RNU. Tỷ lệ sống sót sau 1 và 3 năm của bệnh nhân sau RNU lần lượt là 39,5% và 9,4% [1]. Ở đây, chúng tôi báo cáo về một trường hợp đa di căn, nhưng không biểu hiện PD-L1, UTUC đã được điều trị thành công với liệu pháp đơn trị liệu bằng vắc-xin khối u cố định bằng formalin (AFTV) sau khi thất bại với RNU và hóa trị liệu bổ trợ.
Báo cáo trường hợp
Một bệnh nhân nam 62 tuổi nhập viện với tình trạng đi tiểu ra máu vào tháng 8 năm 2012. Không phát hiện khối u nào trong hệ thống đường tiết niệu bằng siêu âm, và kết quả xét nghiệm tế bào học nước tiểu là loại II (diễn biến lâm sàng của bệnh nhân được minh họa trong hình 1). Một năm sau đó vào tháng 8 năm 2013, cả siêu âm và chụp cắt lớp vi tính (CT) cho thấy có một khối bất thường có kích thước bằng hạt óc chó ở thận phải, được chẩn đoán là ung thư biểu mô đường tiết niệu (Hình 2). Bệnh nhân đã trải qua RNU vào tháng 9 năm 2013. Khối u được phẫu thuật cắt bỏ ở thận phải có màu trắng xám, rắn chắc, ranh giới tương đối rõ và có kích thước 50x50x40 mm. Khối u đã xâm lấn nhu mô thận nhưng chưa đến bề mặt thận. Về mặt mô học, khối u được chẩn đoán là ung thư biểu mô đường niệu có rủi ro cao (p-T3N0) bao gồm các tế bào ung thư có nhân tăng sắc tố và hạt nhân không điển hình mức độ cao. Khối u cho thấy độ dương tính cao tương đối đối với MIB-1 (40%), một chỉ số tăng sinh tế bào (Hình 2, phía dưới bên phải).
Vì các kết quả giải phẫu bệnh học cho thấy tiên lượng xấu nên hóa trị liệu bổ trợ đã được thực hiện với Cisplatin (70mg/m2, ngày 2) và Gemcitabine (1000mg/m2, ngày 1, 8, 15) trong phác đồ 3 tuần. Tuy nhiên, giảm tiểu cầu nghiêm trọng đã tiến triển (CTCAE độ 4). Phác đồ đã được dừng lại sau khi hoàn thành ba đợt hóa trị. Hậu quả là di căn đến phổi và hạch bạch huyết cạnh động mạch chủ (PALN) đã được phát hiện qua chụp CT vào tháng 2 năm 2014, chỉ 5 tháng sau RNU. Bệnh nhân không muốn tiếp tục hóa trị tích cực. Chúng tôi đã giới thiệu AFTV theo yêu cầu của bệnh nhân.
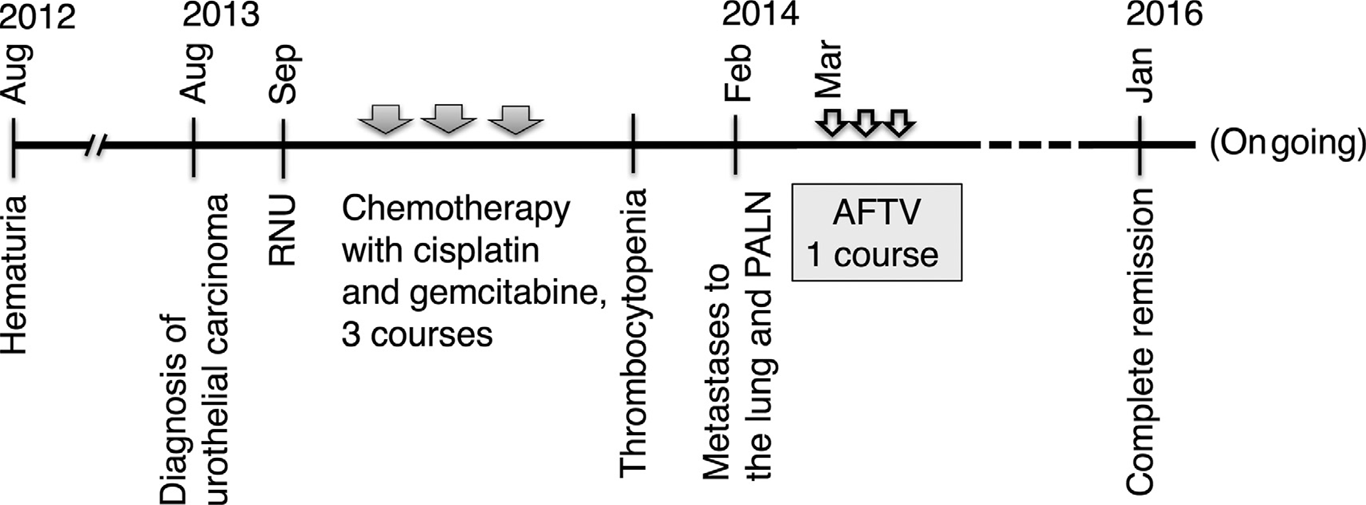
Bảng 1. Diễn biến lâm sàng liệu trình của bệnh nhân. RNU, Phẫu thuật cắt bỏ thận mở rộng; PALN, hạch bạch huyết cạnh động mạch chủ; AFTV, vắc xin khối u tự thân cố định bằng Formalin.

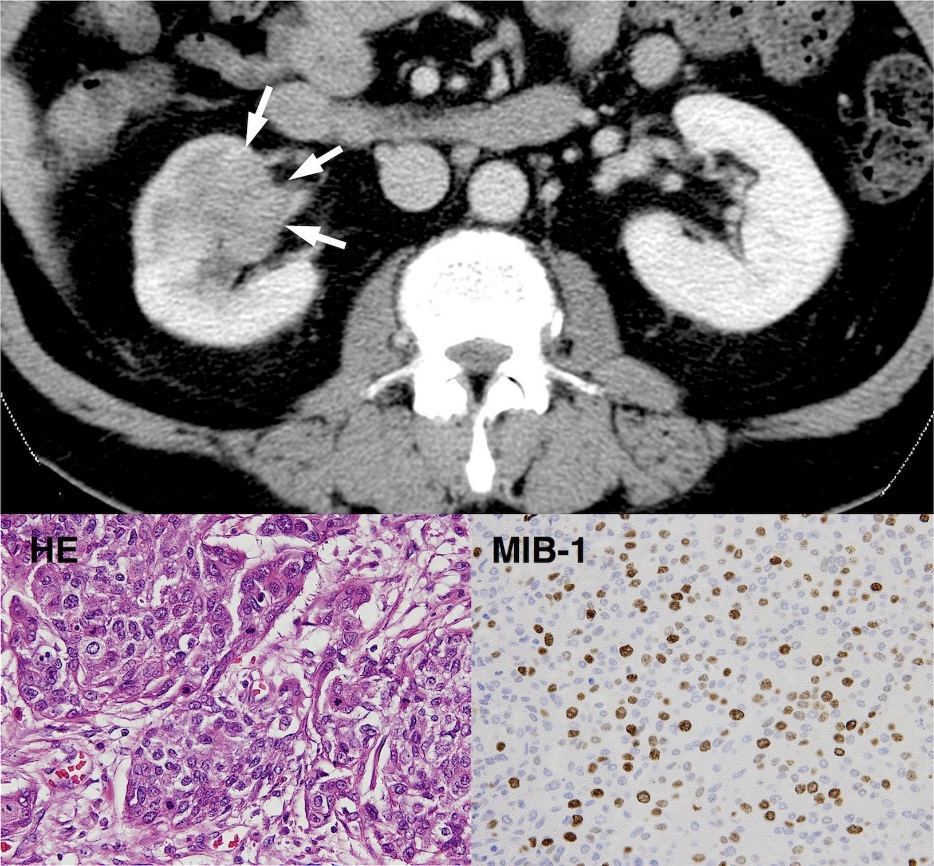
Bảng 2. CT cho thấy một bóng bất thường có kích thước bằng quả óc chó (đường kính xấp xỉ 40 mm) ở thận phải (mũi tên trên đầu). Phía dưới bên trái, nhuộm H&E của mẫu bệnh phẩm đã được cắt bỏ cho thấy ung thư biểu mô tiết niệu xâm nhập với các hạt nhân tăng sắc tố và mức độ không điển hình cao (độ phóng đại, x400). Thấp hơn bên phải, dương tính cao với MIB-1, một chỉ số của sự tăng sinh tế bào.
Để quan sát tình trạng miễn dịch trong khối u trước khi điều trị bằng AFTV, biểu hiện mô bệnh học của HLA A, B, C (MHC-loại I), CD8a, CD4, được lập trình theo phương pháp death-ligand 1 (PD-L1), granzyme B, và hộp đựng P3 (FoxP3) đã được kiểm tra. MHC loại I được biểu hiện mạnh mẽ trên các tế bào khối u cũng như CD8a, CD4 (Hình 3, mặt trên) và granzyme B (Hình 3, mặt dưới), được nhuộm trong các tế bào miễn dịch xâm nhập vào khối u. Ngoài ra, biểu hiện của FoxP3 đã được tìm thấy (đầu mũi tên trong Hình 3, phía dưới bên phải), nhưng biểu hiện PD-L1 đã không được quan sát trên các tế bào khối u (Hình 3, phía dưới bên trái).
Thông qua ban đạo đức của Trung tâm Ginza-Namiki-Dori và sự chấp thuận của bệnh nhân, chúng tôi đã chuẩn bị AFTVac như đã báo cáo [3]. Chúng tôi đã sử dụng 3.4g mô khối u được cố định trong formalin, được cho là chứa các kháng nguyên khối u. Vaccine được tiêm dưới da vào cẳng tay trên của bệnh nhân một lần một tuần, trong 03 tuần, sau giữa tháng 3 năm 2014.
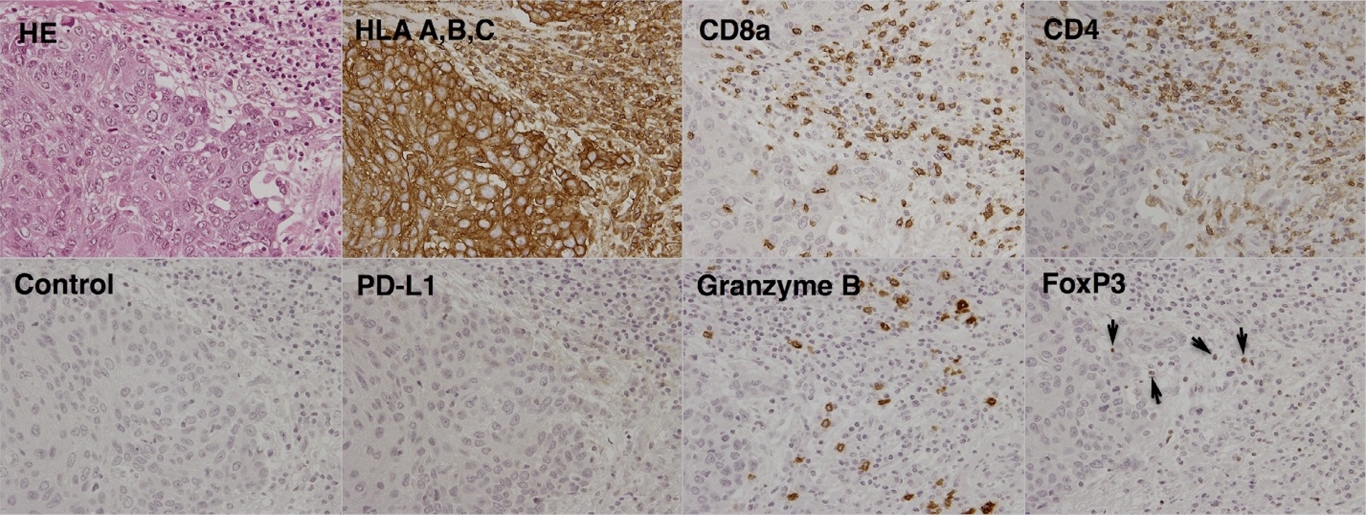
Hình 3. Miễn dịch học, HLA A, B, C (MHC-loại I) được biểu hiện mạnh mẽ trên các tế bào khối u. CD8a, CD4 và granzyme B được nhuộm trong các tế bào miễn dịch trong khối u. FoxP3 đã được thể hiện (đầu mũi tên), nhưng không phát hiện thấy biểu hiện PD-L1 trên các tế bào khối u.

Để đánh giá tình trạng miễn dịch qua trung gian tế bào của bệnh nhân, đáp ứng tăng nhạy cảm loại chậm (DTH) đã được thử nghiệm 2 tuần sau khi tiêm AFTV lần thứ ba (các mô khối u cố định không chứa chất bổ trợ miễn dịch), có kết quả dương tính (nốt ban đỏ có kích thước 30x30 mm và nốt sần cứng 7x7 mm) (Hình 4). Trong quá trình điều trị này, không có tác dụng phụ nào được quan sát ngoại trừ phát ban nhẹ (CTCAE độ 1), xuất hiện tại các vị trí tiêm AFTV cục bộ, dần dần biến mất trong vài tháng.
Chụp chuỗi CT được hiển thị trong hình 5. Nhiều di căn đến phổi và hạch bạch huyết cạnh động mạch chủ đã được phát hiện tại thời điểm tiêm ban đầu. Tuy nhiên, 3 tháng sau, chúng cho thấy xu hướng giảm kích thước. Sau 9 tháng tiếp theo, sự thuyên giảm hoàn toàn ở di căn phổi và giảm hơn nữa ở di căn hạch bạch huyết cạnh động mạch chủ. Hai mươi hai tháng sau, tất cả các di căn đã biến mất trên hình ảnh CT. Kể từ lần tiêm vaccine đầu tiên, 36 tháng đã trôi qua và không thấy có sự tái phát nào. Trong suốt qúa trình này, không có phương pháp điều trị nào khác bao gồm cả chất ức chế điểm kiểm soát miễn dịch.
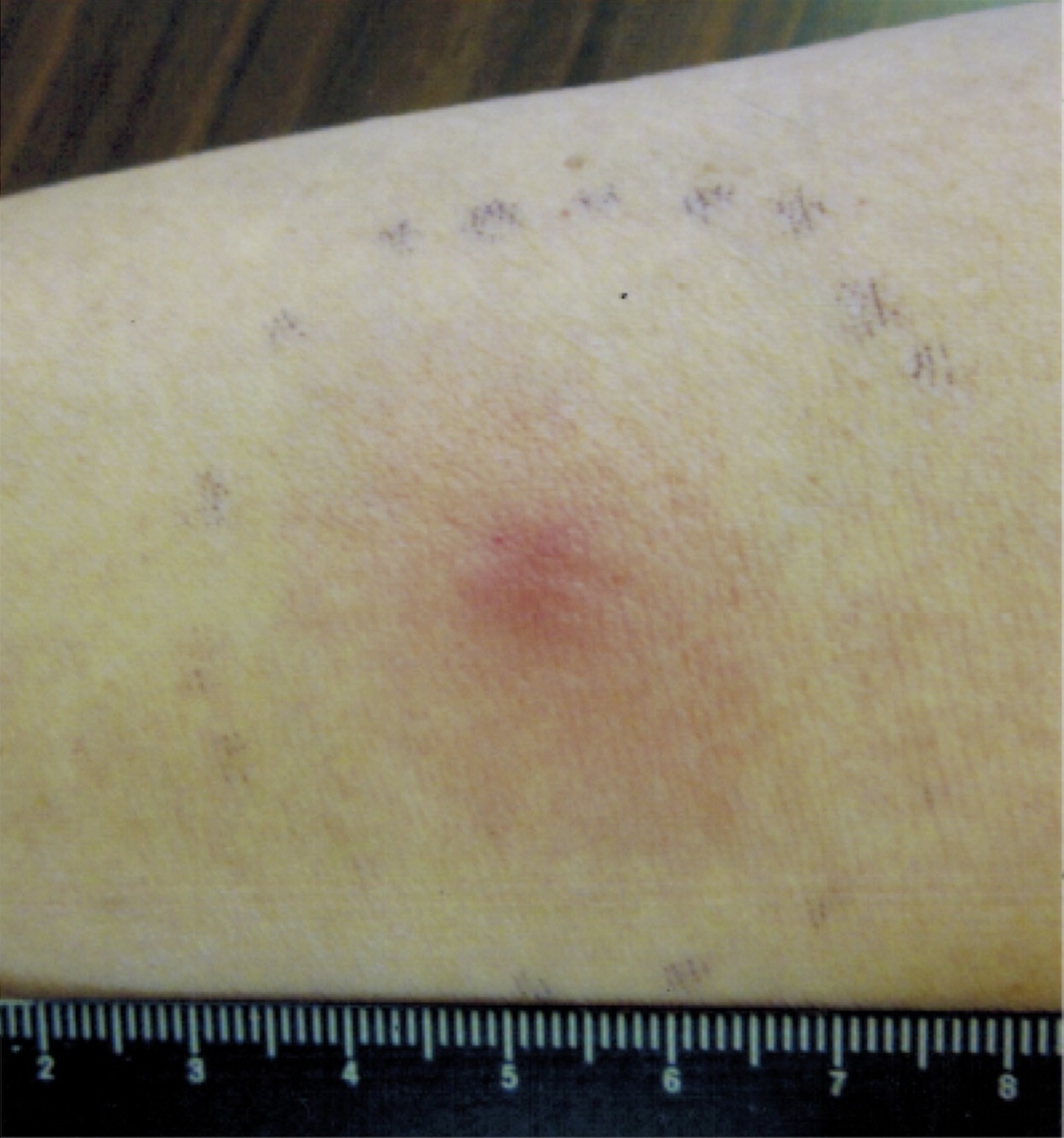
Hình 4. Đáp ứng quá mẫn loại chậm với khối u tự thân cố định trong formalin (mà không sử dụng chất bổ trợ miễn dịch) trở nên dương tính (30x30mm nốt ban đỏ và 10x10mm nốt sần) sau khi tiêm AFTVac lần thứ 3.
Thảo luận
Tiên lượng di căn của ung thư biểu mô đường tiết niệu trên UTUC sau phẫu thuật cắt bỏ thận mở rộng RNU là rất thấp; tỷ lệ sống sót sau 1 và 3 năm phẫu thuật tương ứng là 39.5% và 9.4%, với thời gian sống sót trung bình là 10 tháng [1]. Tái phát là không thể tránh khỏi và không có biện pháp điều trị hữu hiệu. Trường hợp hiện tại là kháng trị liệu với liệu pháp điều trị thông thường (phẫu thuật cắt bỏ thận mở rộng RNU và hóa trị liệu dựa trên platinum), và bệnh nhân rất muốn liệu pháp điều trị mới cho các khối di căn phổi và hạch bạch huyết cạnh động mạch chủ PALN. Bệnh nhân cho thấy đáp ứng hoàn toàn với AFTV mà không có tác dụng phụ đáng kể nào.
Các kết quả hóa mô miễn dịch (Hình 3), có biểu hiện của MHC loại I trên các tế bào khối u và CD8a và granzyme B trên các tế bào miễn dịch trong khối u, cho thấy đáp ứng miễn dịch gây độc chủ động có thể xảy ra chống lại các tế bào khối u. Hơn nữa, PD-L1 âm tính trên các tế bào khối u, cho thấy sự ức chế điểm kiểm soát miễn dịch của PD-L1 có thể không xảy ra trong trường hợp này. Do đó, các tế bào dương tính FoxP3 quan sát thấy trong khối u (thường được cho là bao gồm các tế bào T điều tiết) đã không thể hiện sự ức chế mạnh mẽ hoạt động tiêu diệt của các tế bào T độc (CTL) xâm nhập khối u. Như được hiển thị trong Hình 4, đáp ứng tăng nhạy cảm loại chậm (DTH) dương tính trong trường hợp hiện tại cho thấy rằng CTL đã được tạo ra trên in vivo sau khi tiêm chủng.

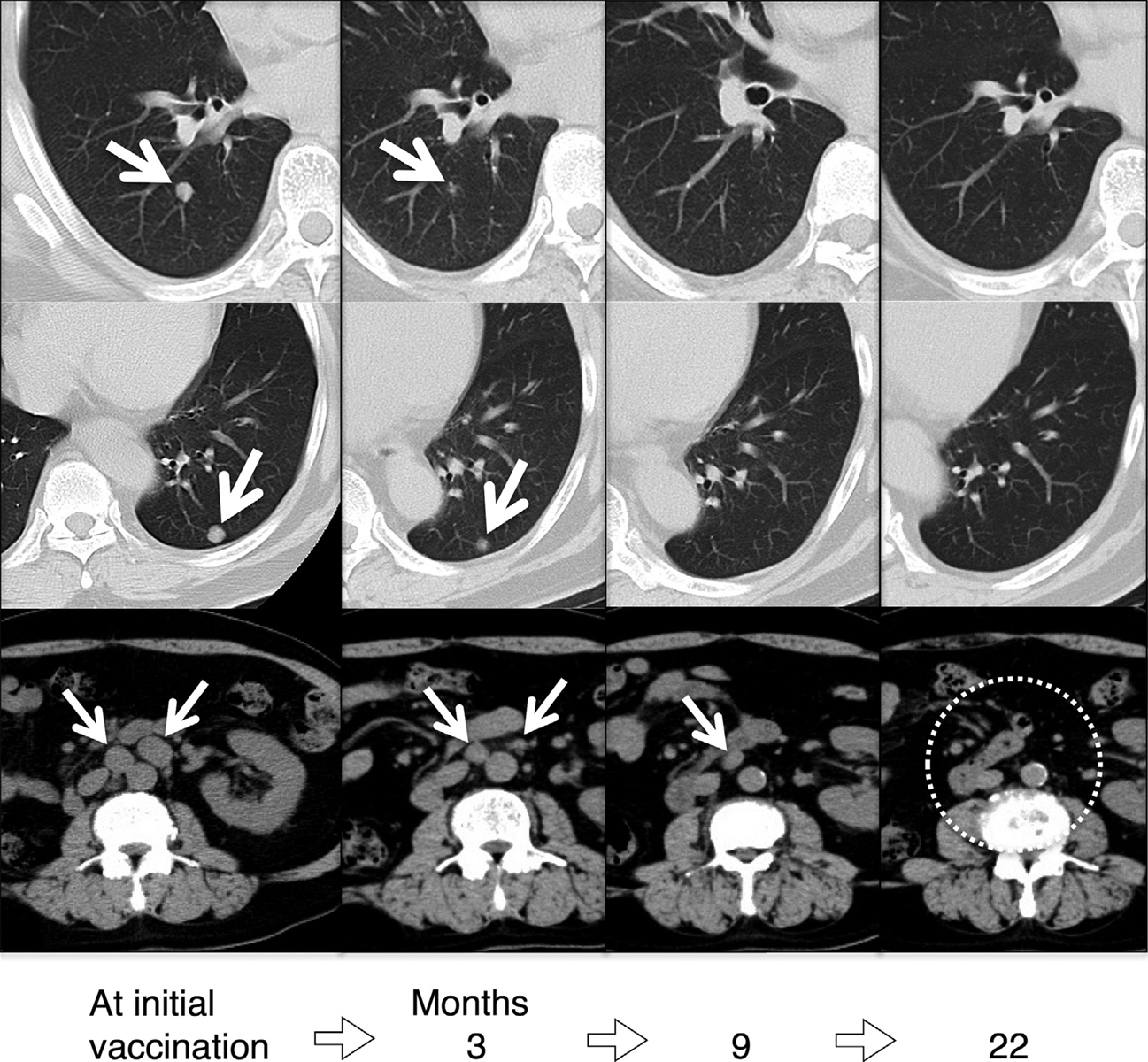
Hình 5.Hình ảnh CT các tổn thương di căn phổi và hạch bạch huyết cạnh động mạch chủ. Nhiều di căn đến các hạch bạch huyết phổi và động mạch chủ được phát hiện ở thời điểm tiêm vắc-xin mũi đầu tiên với AFTV. Ba tháng sau lần tiêm chủng đầu tiên với AFTV, tất cả các tổn thương di căn cho thấy xu hướng giảm kích thước. Chín tháng sau khi tiêm vắc-xin đầu tiên với AFTV, sự biến mất của di căn ở phổi và giảm hơn nữa di căn hạch bạch huyết động mạch chủ đã được phát hiện. Hai mươi hai tháng sau, hình ảnh tất cả các di căn đã biến mất.
Chúng tôi đã báo cáo trước đây về tác dụng dự phòng của AFTV (một liệu trình, tức là ba lần tiêm
chủng như đã đề cập cho trường hợp hiện tại, đủ để tạo ra phản ứng DTH) để ngăn chặn sự tái phát thường xuyên của ung thư biểu mô tế bào gan (HCC) trong một thử nghiệm ngẫu nhiên [4], trong trường hợp tái phát HCC, trong đó AFTV khiến tế bào lympho T (CTL) gây độc đặc hiệu glypican-3 [5] và một trường hợp HCC tái phát nhiều lần đã được điều trị 29 lần với các phương thức khác nhau, bao gồm ba lần phẫu thuật nội soi [6]. Một hiệu quả điều trị điển hình của AFTV cũng được quan sát thấy trong việc loại bỏ ung thư biểu mô tuyến vú di căn xương [7]. Quan trọng hơn, chúng tôi đang nghiên cứu các tác dụng lâm sàng của AFTV ở những bệnh nhân mới được chẩn đoán bệnh đa u nguyên bào thần kinh đệm (GBM) mà không thể cắt bỏ hoàn toàn được. Trong khi liệu pháp tiêu chuẩn hiện tại đối với GBM mới được chẩn đoán có thời gian sống trung bình (mOS) là 14,6 tháng [8], mOS đã đạt 22,2 tháng trong một thử nghiệm lâm sàng của chúng tôi [9]. Những bệnh nhân cho thấy phản ứng DTH dương tính với các mảnh khối u GBM tự thân cố định bằng formalin (không có miễn dịch bổ trợ) sau khi tiêm vắc-xin AFTV đã sống sót lâu hơn so với những người có phản ứng DTH âm tính (P = 0,0071, xét nghiệm rank-log) [9]. Do đó, chúng tôi kết luận rằng AFTV có thể cung cấp cả kháng nguyên đặc hiệu và kháng nguyên khối u cụ thể cho từng bệnh nhân.
Mặc dù, hiển nhiên, các nghiên cứu sâu hơn trong một thử nghiệm lâm sàng quy mô lớn hơn là cần thiết để xác nhận kết quả của chúng tôi, nhưng trường hợp hiện tại đưa ra cái nhìn đầu tiên vô cùng hấp dẫn về sự đóng góp tiềm năng của liệu pháp miễn dịch bằng AFTV.
Kết luận
Liệu pháp vaccine ung thư như AFTVac có thể thích hợp cho ung thư biểu mô đường tiết niệu trên di căn UTUC đã kháng trị liệu với hóa trị, nếu khối u âm tính với PD-L1.